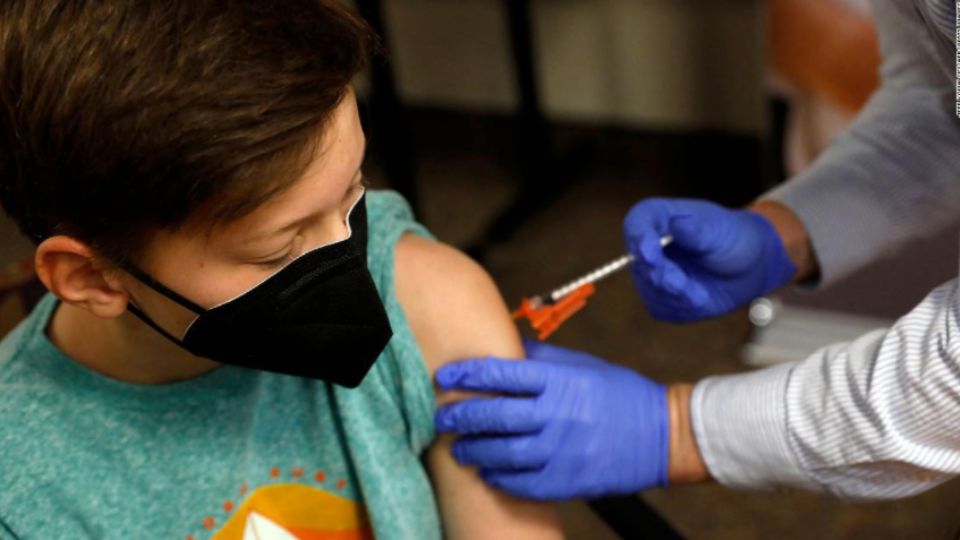
Este miércoles, la farmacéutica Moderna ha indicado buscar la autorización para su vacuna covid en niños pequeños de seis meses a cinco años, luego de demostrar en sus ensayos clínicos la eficacia de esta.
Te podría interesar
La investigación involucró a 11 mil 700 niños en Estados Unidos y Canadá, 4 mil 200 de ellos con edades de entre dos y seis años y 2 mil 500, de entre seis meses y dos años.
Se tratan de dos dosis de 25 microgramos administradas a menores de edad en esta franja de edad. Según el reporte de la empresa, las inyecciones produjeron niveles de anticuerpos similares a los niveles alcanzados por dos dosis de 100 microgramos en jóvenes de 18 a 25 años.
Stephane Bancel, director ejecutivo de Moderna, se mostró sumamente entusiasmado por los resultados, reportando estos nuevos datos mediante un comunicado oficial.
"Son buenas noticias para los padres de niños menores de seis años. Ahora tenemos datos clínicos sobre el rendimiento de nuestra vacuna desde en niños de seis meses hasta en adultos mayores" comentó Stephane Bancel en el comunicado.
A pesar de los excelentes resultados con la covid-19, no se pudo decir lo mismo con la variante Ómicron, registrando una eficacia relativamente baja con respecto a los contagios durante la ola de dicha cepa, mostrando una efectividad de 43.7% en niños de seis meses a dos años y de 37.5% en los de dos a cinco años.
Moderna reveló dichos resultados, comparados con los hechos en adultos y mostrando el mismo comportamiento. Actualmente se está evaluando una tercera dosis para incrementar su eficacia.
El mes pasado, la Agencia de Medicamentos de Estados Unidos (FDA) postergó sus debates sobre la licencia de la vacuna de Pfizer-BioNTech para menores de cinco años, argumentando necesitar datos adicionales sobre la tercera dosis.
Las compañías aseguraron tener listos estos datos para abril. Mientras tanto, Moderna presentará la solicitud tanto para el órgano regulador de Estados unidos, como a la Agencia Europea de Medicamentos (EMA) y otros reguladores.
La búsqueda de Moderna para la autorización de su vacuna covid en niños pequeños, busca también proteger a este sector de la población.
Jesús García